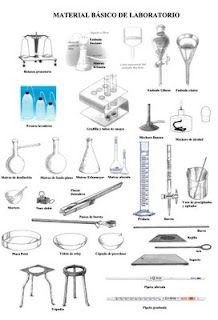
Los elementos de laboratorio se dividen en :
- Elementos de vidrio
- Elementos de diferente material que son de vidrio
Elementos de vidrio :
- Varilla
- Vaso de precipitados
- Probeta
- Erlenmeyer
- Vidrio reloj
- Vaso de petri
- Tubo de ensayo
- Pipeta
- Ampolla de Bater
- Embudo
Varilla : Esta compuesta de vidrio maciso o hueco en su parte central , se utiliza para mezclar sustancias , puede ser reemplazado por una varilla de plástico macizo.
Vaso de precipitados : Se utiliza para disolver, mezclar , o hacer reaccionar sustancias , esta compuesta de un vidrio especial templado para poder ser utilizado sobre la fuente de calor . E general presenta un logo que puede ser blanco o amarillo. Es graduado , sirve para medir .
Probeta : Es de vidrio , posee una base de apollo , es graduado y no se puede someter a la acción del calor y se utiliza para medir volúmenes de sustancias liquidas .
Erlenmeyer : Base plana , es de vidrio , se puede someter a la acción del calor , presenta el logo de graduado , presenta un cuello largo y se utiliza para calentar sustancias que emanan vapores , que no puede estar en contacto con el aire.
Vidrio reloj : No se puede someter a la acción del calor y se utiliza para mezclar pequeñas cantidades de sustancia solida.
Caja de petri : Es de vidrio , transparente , se utiliza como germinador , para cultivos de hongos y bacterias y no puede ser sometida a la acción del calor .
Pipeta : Es de vidrio graduado , y sirve para tras basar con un volumen exacto de un recipiente al otro .
Ampolla de bater : Sirve para separar dos líquidos no visibles , como el agua y el aceite , poseen una marinela la cual permite el paso del agua , y en la ampolla queda el aceite.
Embudo : Es de vidrio y sirve para filtrar , puede ser reemplazado por uno de plástico .
Tubo de ensayo : Es de vidrio , se puede someter al calor , presenta el logo y se utiliza para mezclar o hacer reaccionar sustancias.
Elementos que no son de vidrio :
- Gradilla
- Broche
- Cuchara/Espátula
- Mortero y Pilón
- Cápsula
- Soporte metálico
- Mechero de Bunsen
- Tela de amianto
- Papel de filtro
- Trípode
Gradilla : Puede ser de metal , de plástico o de madera y se utiliza para sujetar a los tubos de ensayo , en general se pueden hacer seis de lado a lado .
Broche : Se utiliza para sujetar a los tubos de ensayo , cuando tienen que ser sometidos a la acción del calor , poseen un brazo mas largo la cual impide que las personas se quemen .
Cuchara/Espátula : Se utiliza para extraer pequeñas cantidades de sustancias solidas .
Mortero y Pilón : Puede ser de madera , de porcelana o de plástico duro y se utiliza para machacar sustancias solidas o las que hay que extraer sus jugos .
Cápsula : Es de porcelana , se puede someter a la acción del calor y se utiliza para ser reaccionar cantidades de sustacias solidas o solidas y liquidas .
Soporte metálico : Es de metal , y posee un aro donde se ubica la ampolla de bater .
Mechero de Bunsen : Es la fuente de calor ultilizada en el laboratorio .
Tela de amianto : Se coloca sobre el Trípode , esta tela sirve para distribuir el calor de forma pareja .
Papel de filtro : Es un disco de papel el cual se utiliza para colocarlo dentro del embudo y retener sustancias solidas .
Trípode : Limpia y cubre objetos , se utiliza para poder observar al microoscopio , sobre el portaobjetos , se coloca el material sobre el portaobjetos .